Volume 40 - numÉro 14 - 5 dÉcembre 2005 |
|
||
Année internationale de la physiqueLe nanoballon et la valse des électrons
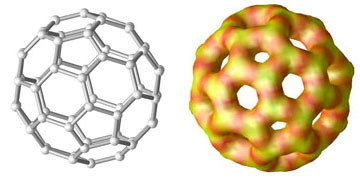
L’année 1985 a été le théâtre d’une petite révolution en physique et en chimie: la découverte, par Curl, Kroto et Smalley, de la très élégante molécule C60, qui allait procurer à ses auteurs, à peine 10 ans plus tard, un prix Nobel et surtout ouvrir toute grande la porte de la recherche sur les matériaux dits «exotiques»! Véritable rupture avec les matériaux traditionnels, ces matériaux nouveaux prennent des formes inattendues et leurs propriétés sont parfois étonnantes. La molécule C60 est, comme son nom l’indique, constituée de 60 atomes de carbone. Elle ressemble à s’y méprendre à un ballon de soccer. Si l’on examine un tel ballon, on constate qu’il est composé exclusivement de pentagones et d’hexagones, qui sont assemblés de façon hautement symétrique. Au 18e siècle, le grand mathématicien Euler a démontré que, pour former une sphère en n’utilisant que des pentagones et des hexagones, il fallait utiliser exactement 12 pentagones – pas un de plus, pas un de moins. Le ballon de soccer est le plus simple arrangement où aucun des pentagones ne se touche. C’est sans doute pour cette raison que ceux qui ont conçu ce ballon en sont arrivés à cette forme, et il semble que la nature ait fait le même raisonnement… il y a beaucoup plus longtemps! Le nombre de nœuds (les points d’intersection entre les arêtes des polygones) à la surface du ballon est égal à 60. Si l’on place un atome de carbone à chacun des nœuds, on obtient une molécule C60 – à une «petite» différence près: le diamètre d’un ballon de soccer est d’environ 30 cm alors que la molécule C60 a un diamètre de 0,7 nanomètre, soit moins de un millionième de millimètre! Pour donner une idée de cette différence de grandeur, le rapport est à peu près le même qu’entre la Terre et une fourmi! On a donné le nom de fullerène à cette molécule dont la structure rappelle les dômes géodésiques du célèbre architecte Richard Buckminster Fuller; tout près de chez nous, sur l’île Sainte-Hélène, la Biosphère en est un très bel exemple. Cette petite molécule a bouleversé la recherche en science des matériaux. En regroupant suffisamment de ces fullerènes, il est possible de former un solide qui ressemble en tous points à un solide traditionnel, parfaitement ordonné, à la manière de briques formant un mur. Ce solide de C60 est isolant, c’est-à-dire qu’il ne conduit pas l’électricité. Il est possible de le rendre métallique, ou conducteur, en introduisant des atomes alcalins (du potassium par exemple) entre les molécules. Propriété intéressante, ce métal devient supraconducteur – il n’offre donc plus de résistance au courant électrique – lorsqu’on abaisse sa température à environ 40º du zéro absolu, soit -230 ºCelsius. Elle est encore bien loin de nos grands froids d’hiver, mais cette température est quand même parmi les plus élevées où la supraconductivité se manifeste… pour le moment! Un courant électrique est un flot d’électrons qui se déplacent dans un matériau. Dans un métal normal, le mouvement des électrons est restreint par des collisions avec les atomes et les autres électrons; c’est ce qui produit la résistance au passage du courant électrique. Dans un supraconducteur, les électrons forment des paires et peuvent se déplacer ainsi sur de grandes distances. On pourrait comparer les mouvements des électrons à une grande valse où chaque couple effectue des pas différents de ceux des autres, tout en se déplaçant sur la piste sans jamais heurter les autres couples. En poussant plus loin cette analogie, un métal normal ressemblerait davantage à une fête techno! La fabrication de matériaux supraconducteurs à des températures plus «utilisables» est l’un des grands défis de la physique. La molécule C60 fera peut-être partie de la solution; les chercheurs du Département de physique et ceux du Département de chimie ne négligent aucun effort pour y arriver, faisant appel à une vaste panoplie de méthodes aussi bien expérimentales que théoriques. On imagine facilement l’intérêt pour les réseaux de transport électrique si l’on découvrait des matériaux qui «supraconduisent» même durant les grandes canicules de juillet! Michel Côté |
|||
Ce site a été optimisé pour les fureteurs Microsoft Internet Explorer, version 6.0 et ultérieures, et Netscape, version 6.0 et ultérieures.